6款新药陆续获批,七月审批速度依旧给力
据FDA官网2018年8月1日提供的最新公布结果,FDA在2018年7月已经陆续批准了6款新药,这也是2018年来批准新药最多的一个月份(五月也是批准了6款新药)。
2017年是美国药物批准的大年,美国食品和药物管理局(FDA)批准了46种新药以及两款CAR-T疗法、一款基因疗法。2018年也会是批准的大年吗?从趋势来看,2018年依旧会有较多新药获批,在已过去的七个月中已有26款新药获批,包括21个新分子实体和5个新生物制品,预计能够有超过40款新药获批。
图1:美国CDER1997-2017年批准的新药数量
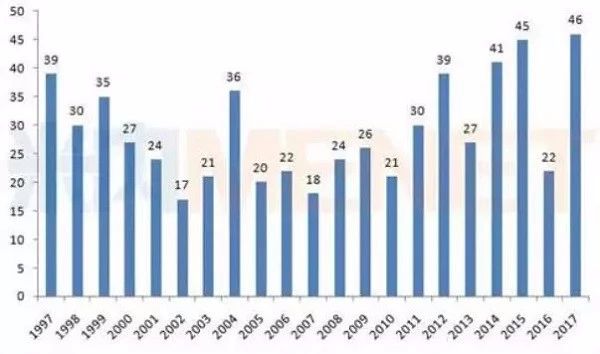
6款新药陆续获批,涉及多个疾病领域
表1:2018年7月获批新药的情况
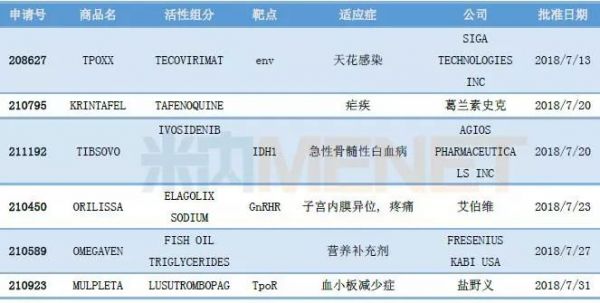
获批的6款新药均属于新分子实体,涉及多个疾病领域。作为2018年下半年首款获批的新药TPOXX(tecovirimat),是首款在FDA获批用于治疗天花的药物。防患于未然,警惕天花卷土重来。TIBSOVO(Ivosidenib)是FDA今年批准的第五款癌症新药,用于治疗急性骨髓性白血病,是全球首款获批的IDH1抑制剂,具有重磅药物潜力。Orilissa(Elagolix)是FDA批准的首个治疗子宫内膜异位症中重度疼痛的口服药物,极具潜力。多款新药陆续获批,给美国患者带来了新的治疗选择,也给相应公司带来了诸多利好。
1.未雨绸缪,首款治疗天花的药物:TPOXX(tecovirimat)
2018年7月13日,美国FDA宣布批准SIGA Technologies的新药TPOXX(tecovirimat)上市,用于治疗天花。值得一提的是,这是美国FDA今年批准的第21款新药,也是首款获批治疗天花的新药。
图2:Tecovirimat的分子结构式
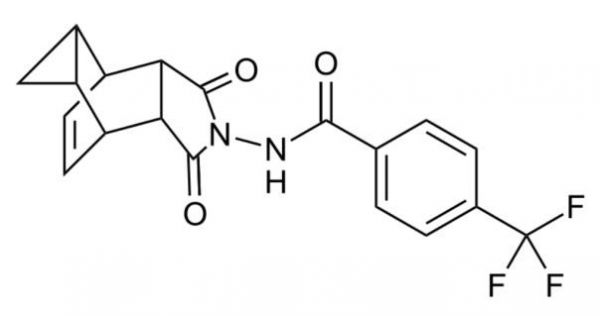
尽管世界卫生组织宣布天花作为一种可能致命的传染病于1980年被根除,但长期以来人们一直担心天花可能被用作生物武器。为解决生物恐怖主义的风险,美国国会已采取措施,批准阻止被用作武器的病原体的对策。此次TPOXX 的获批上市是一个重要里程碑。未雨绸缪,防患于未然,希望未来能有更多这类新药获批。
2.60年首款间日疟疾新药:Krintafel(tafenoquine)
2018年7月20日,美国FDA宣布批准葛兰素史克的新药Krintafel(tafenoquine,他非诺喹),用于正在接受适当抗疟药物治疗急性间日疟原虫(P.vivax)感染的16岁及以上疟疾患者,根治(预防复发)由间日疟原虫(P.vivax)导致的疟疾。他非诺喹由美国沃尔特·里德陆军研究所(WRAIR)的科学家于1978年首次合成,这是一种8-氨基喹啉衍生物,具有抗间日疟生命周期的活性,包括位于肝脏中的休眠形式的间日疟原虫。GSK与MMV早在2008年就达成了战略合作,历时十年开发出这款抗疟新药。
图3:Tafenoquine分子结构式
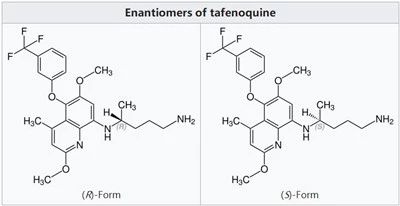
FDA通过优先审查程序对Krintafel进行了审批,还授予了突破性药物资格。此次批准也使Krintafel成为过去60多年来治疗间日疟原虫疟疾的首个新药,该药能够有效预防间日疟复发,对于患有这种疟疾的患者群体而言是一个里程碑。在批准Krintafel的同时,FDA还颁发给GSK一张热带疾病优先审评券,以奖励其在被忽视热带病药品研发方面做出的贡献。
3.首款IDH1抑制剂:TIBSOVO(Ivosidenib)
2018年7月20日,美国FDA宣布批准Agios Pharmaceuticals的重磅抗癌新药TIBSOVO(Ivosidenib),用于经一款检测方法(雅培RealTime IDH1伴随诊断试剂盒)证实存在易感异柠檬酸脱氢酶-1(IDH1)突变的复发性或难治性急性髓系白血病(R/R AML)成人患者。TIBSOVO是一种IDH1酶的口服靶向抑制剂,是目前唯一一款获得美国FDA批准针对IDH1突变的R/R AML疗法。此次Tibsovo获批,对于基石药业也是大好消息。今年6月底,基石药业与Agios签署独家合作与授权协议,获得Tibsovo在大中华区的独家权利。基石药业将负责Tibsovo在大中华区针对血液肿瘤和实体瘤适应症的临床开发和商业化,并将首先专注于AML及胆管癌。
图4:Ivosidenib的分子结构式
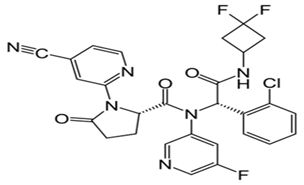
Tibsovo是一款同类首创的、具有选择性的、针对IDH1基因突变癌症的强效口服靶向抑制剂。IDH1是一种代谢酶,其基因突变存在于包括AML、胆管癌和神经胶质瘤在内的多种肿瘤。除了AML之外,Agios公司也正在评估Tibsovo用于携带IDH1突变的新诊AML、胆管癌、低级别神经胶质瘤的潜力。良好的疗效,突破性的疗法,使得该药深受关注,预计未来五年全球销售额峰值能达到近10亿美元。
4.10年来新突破,子宫内膜异位症新药:ORILISSA(elagolix)
2018年7月20日,美国FDA宣布批准艾伯维的重磅新药ORILISSA(elagolix),用于女性患者子宫内膜异位症相关的中度至重度疼痛的治疗。这是目前唯一一款口服促性腺激素释放激素(GnRH)拮抗剂,也是十年来首个获FDA批准用于该适应症的口服疗法。ORILISSA是一种口服GnRH拮抗剂,通过抑制脑垂体促性腺释放激素受体,最终降低血循环中性腺激素水平。给药会对黄体生成素和卵泡刺激素产生剂量依赖性抑制,降低卵巢性激素、雌二醇和黄体酮的血药浓度,最终达到控制疼痛的效果。
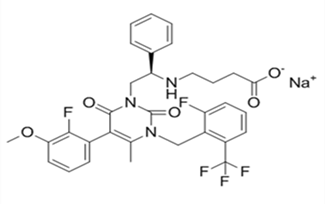
图5:Elagolix的分子结构式
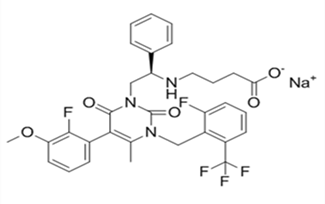
子宫内膜异位症是美国最常见的妇科疾病之一。据估计,全球每10名育龄女性中就有一人患有这种疾病,数量大约有1.76亿患者。它可能产生使人衰弱的疼痛,通常可以通过口服避孕药、非甾体类抗炎药(NSAIDs)、阿片类药物和激素疗法等进行治疗,这些药物对某些女性有效,但很少有特别适用于子宫内膜异位症的治疗。在更多的病例中,患者经常需要接受手术干预,但手术无法为所有患者带来治愈效果。因此,这一领域还有巨大的医疗需求亟待满足。作为10多年来首个治疗子宫内膜异位症相关疼痛的口服新药,业界对其的商业前景非常看好,预计该药未来五年销售额峰值能达到12亿美元。
5.营养补充剂:Omegaven(fish oil triglycerides)
2018年7月27日,美国FDA宣布批准Omegaven(fish oil triglycerides)上市,作为罹患“肠外营养相关胆汁淤积”的儿童患者的卡路里与脂肪酸补充剂。由Fresenius Kabi公司带来的Omegaven就是一款充满潜力的新疗法。它由鱼油组成,且主要内容物为omega-3脂肪酸。在动物实验中,研究人员们发现静脉注射鱼油能缓解胆汁淤积的病情。因此,这款疗法有望能在人体中达到同样的效果,在提供营养的同时,逆转患者的病情。在欧洲,Omegaven在多年前就已获批上市。而随着美国FDA的批准,这款新疗法有望来到更多患儿身边,改善他们的病情,让他们度过生命早期的难关。
6.血小板减少症:Mulpleta(lusutrombopag)
2018年7月31日,美国FDA宣布批准盐野义的Mulpleta(lusutrombopag)上市,用于改善慢性肝病患者中血小板减少症。这是一款口服的人类血小板生成素(TPO)受体激动剂,能与巨核细胞表面的TPO受体相结合,诱导这些细胞的增殖、分化、与成熟,从而上调血小板的产生。这款创新疗法已于2015年9月28日获得日本的批准,在选择进行侵入性手术的慢性肝脏疾病患者中,改善他们的血小板减少症病情。该药的获批给患者带来新的治疗选择,不过由于相关病人数量过于稀少,该药的销售前景并非一片光明,预计未来五年销售额峰值仅能突破千万美元。
图6:Lusutrombopag的分子结构式
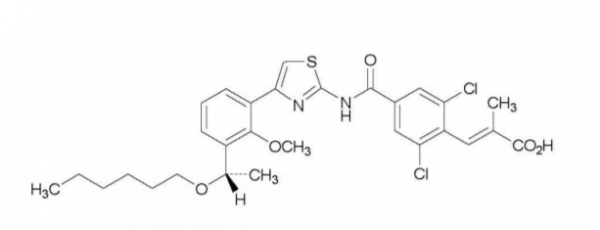
结语创新驱动进步,新药的获批意味着患者有更多的治疗选择。随着国内对药物研发的重视,各种激励政策的实施和各大药企的不断增加研发投入,在各大疾病领域新药开发中出现了越来越多国内企业的身影。同时也有一些优秀的国内创新药企正在积极布局国际市场,相信在未来几年将会有国产新药在FDA获得批准,创造中国药物研发的历史。
责任编辑:露儿
-
一批药被查 涉维C银翘片、阿胶…
一批药被查 涉维C银翘片、阿胶…...
-
高值耗材最高降价80% 涉雅培、波科、贝朗…
8月1日,云南省曲靖市举行高值医用耗材联盟带量集中采购第一批次中选产品企业签约仪式。...
-
国家指令 整治所有医院回扣 暗访组出发
日前,国家卫健委发布了《2020年医疗行业作风建设工作专项行动方案》,这次方案的重点就是规范医疗机构及其从业人员行为,印发给各省、自治区、直辖市及新疆生产建设兵团卫生健康委,开始组织实施。...
-
医药代表系统学习产品知识的十个步骤
每个刚入行的医药代表初期都会接受公司大量培训,产品知识培训更是重中之重,不仅培训而且还要考试。...
-
“3+6”医用耗材带量采购,价格信息公布
吉林省政府采购中心消息发布《京津冀及黑吉辽蒙晋鲁医用耗材(人工晶体类)联合带量采购文件(LH-HD2020-1)》(下称《采购文件》),公布人工晶体类耗材的具体采购品种、申报价格等信息。 ...
-
首轮价格降幅低于42% 医疗器械企业直接淘汰
首轮价格降幅低于42% 医疗器械企业直接淘汰...
-
Q1最惨淡的两大药品领域,代表都离职了!
中国虽然是世界上最先控制住疫情的国家,但随着全球疫情的爆发,输入病例不断上升,加上中国本土还有不少无症状感染患者,这使得中国经济无法完全恢复正常。...
-
某些药企又要开启新一轮裁员了
做代表难,今年更加难。除了国家级的带量采购,省级也有带量采购,感觉就像是夹缝中求生存。...
-
两家外企大裁员,患教专员全部解散!
两家外企大裁员,患教专员全部解散!...
-
执业药师挂证,面临终生逐出行业的巨大风险
执业药师挂证,面临终生逐出行业的巨大风险...
-
虚开发票2.5亿,涉多家药械企业(附目录)
近日,国家税务总局马鞍山市税务局发布的《重大税收违法案件信息公告2020年3月》显示,51家企业涉嫌虚开发票,其中24家是药械企业或相关资讯、服务企业。...
-
91家药企收入公开:以岭、科伦、康恩贝…
突如其来的新冠肺炎疫情,对中国的冲击力和冲击面都超过了2003年的非典,对中国经济乃至世界经济也产生了不可避免的影响,也严重扰乱了正常的经济运行节奏。...





















