盘点:2014年9月份FDA审批药物亮点
核心提示:2014年9月份美国FDA共审批通过13个新药,1类新分子实体药物2个,新生物药物2个,3类新剂型药物4个,4类新组合物药物1个,5类新规格或新生厂商药物3个,6类新适应症药物1个。
2014年9月份美国FDA共审批通过13个新药,1类新分子实体药物2个,新生物药物2个,3类新剂型药物4个,4类新组合物药物1个,5类新规格或新生厂商药物3个,6类新适应症药物1个。
表1 2014年9月份美国FDA审批通过新药
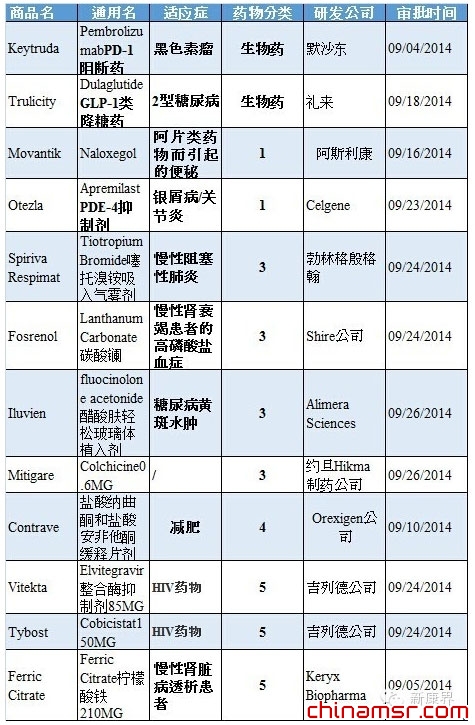
注:数据来源:根据FDA网站统计整理
药物分类:1类新分子实体;3类新剂型;4类新组合物;5类药物新规格或新生商;6类新适应症
黑色素瘤生物药Pembrolizumab
2014年09月04日美国FDA审批默沙东公司研发的黑色素瘤生物药Pembrolizumab(商品名Keytruda)上市。Pembrolizumab是抗PD-1(programmed death 1,程序性死亡-1受体) 人源化单克隆抗体药物,治疗已经接受过Ipilimumab治疗但仍有进展,或对Ipilimumab和BRAF抑制剂双重耐药的BRAF V600基因变异的晚期黑色素瘤患者。
2012年,Pembrolizumab在美国被授予孤儿药资格用于IV期恶性黑色素瘤的治疗,2013年Pembrolizumab在美国被授予突破性治疗药物资格用于晚期恶性黑色素瘤的治疗。2014年,Pembrolizumab在日本孤儿药也被授予孤儿药资格用于恶性黑色素瘤的治疗。
2型糖尿病GLP-1类新药Dulaglutide
2014年09月18日美国FDA审批礼来公司的2型糖尿病Dulaglutide(商品名trulicity)上市。Dulaglutide是GLP-1(胰高血糖素样肽-1)受体激动剂类药物,这是继诺和诺德的利拉鲁肽(liraglutide),百时美施贵宝和阿斯利康的艾塞那肽(Exenatide),以及赛诺菲的利西拉肽(Lyxumia)、葛兰素史克阿必鲁肽(Albiglutide)后美国FDA批准的又一个GLP-1受体激动剂类降糖药。
阿片类药物引起的便秘治疗新药Naloxegol
2014年09月16日美国FDA审批阿斯利康公司研发的1类新分子实体药物Naloxegol(商品名Movantik)上市,用于治疗阿片类药物引起的便秘。
银屑病/关节炎新药Apremilast
2014年09月23日美国FDA审批Celgene公司研发的1类新分子实体药物Apremilast(商品名Otezla)上市,用于治疗银屑病和关节炎。Apremilast是PDE-4抑制剂((phosphodiesteras-4抑制剂,磷酸二酯酶-4抑制剂)。
责任编辑:露儿
-
医院新规:查医药代表 挂钩产品
大医院严查医械代表再升级!私下接触医务人员,直接停止采购公司代理产品。...
-
编外人员被收保证金?医院取消编制大势所趋
看到一家县级医院向编外人员收取5000元工作保证金,限时不交清者,医院不再使用,老徐认为:编制制度或早已不适应医院发展需要了。...
-
三甲医院:8个药询价 要求至少稳定供货半年
三甲医院:供货不稳定,踢出一年。...
-
5省497名执业药师挂证被查实
今年“3•15”后,执业药师“挂证”问题引起全社会关注,按照国家药监局要求,自2019年5月1日起,各省级局组织对行政区域内的药品零售企业开展监督检查。...
-
又一大药陷入致癌风波 多家外企全球召回产品!
一些雷尼替丁药物又被查实含有NDMA杂质,目前山德士、葛兰素史克、印度瑞迪博士药厂均已停止雷尼替丁的供应并召回!...
-
大洗牌!国务院检查组,进入医疗器械企业了
国家严惩在医疗器械购买、销售、纳税...等多个环节的违规情况。...
-
4+7全国扩围,中标结果流出
大跌眼镜!4+7全国扩围结果出炉,有外企低价入围,部分原中选药企落标,多个品种再次刷新底价!...
-
国务院发文:医械行业,筛选重点企业监管
当监管方式越来越科学,不合规或打擦边球的械企面临的压力就越来越大。...
-
报告显示:多数医生不再愿意接待医药代表
报告显示,医生不再愿意接待医药代表,医药代表的必要性在降低。...
-
750家医药企业,最新离职率公布
2019年1月到6月的市场薪酬数据白名单公布,其中医药行业的行业增长和薪酬增长都维持稳定的高位;此外,报告采集了750家医药公司的数据,医药人的平均离职率仅为5.91%,为所有行业中最低的。...
-
63个药,底价曝光(附名单)
(9月6日),山东省药品集中采购网发布《关于山东省药品集中采购拟备案采购产品最低外省及拟挂网价格公示的通知》(以下简称《通知》)。...
-
医药业平均月薪公布 仍是最好的就业去向之一
据东方财富Choice数据,医药行业平均月薪为1.03万,同比涨幅较大,为11.75%,仅次于公用事业等行业,排名第六名。...





















